Fritz Habers große Erfindung - wird Ammoniak heute noch synthetisch hergestellt?
Wie ging es mit der Ammoniaksynthese weiter? Welche Umweltschäden treten durch die Verwendung von Kunstdünger auf? Was machen die Erben heute im Fritz-Haber-Institut?
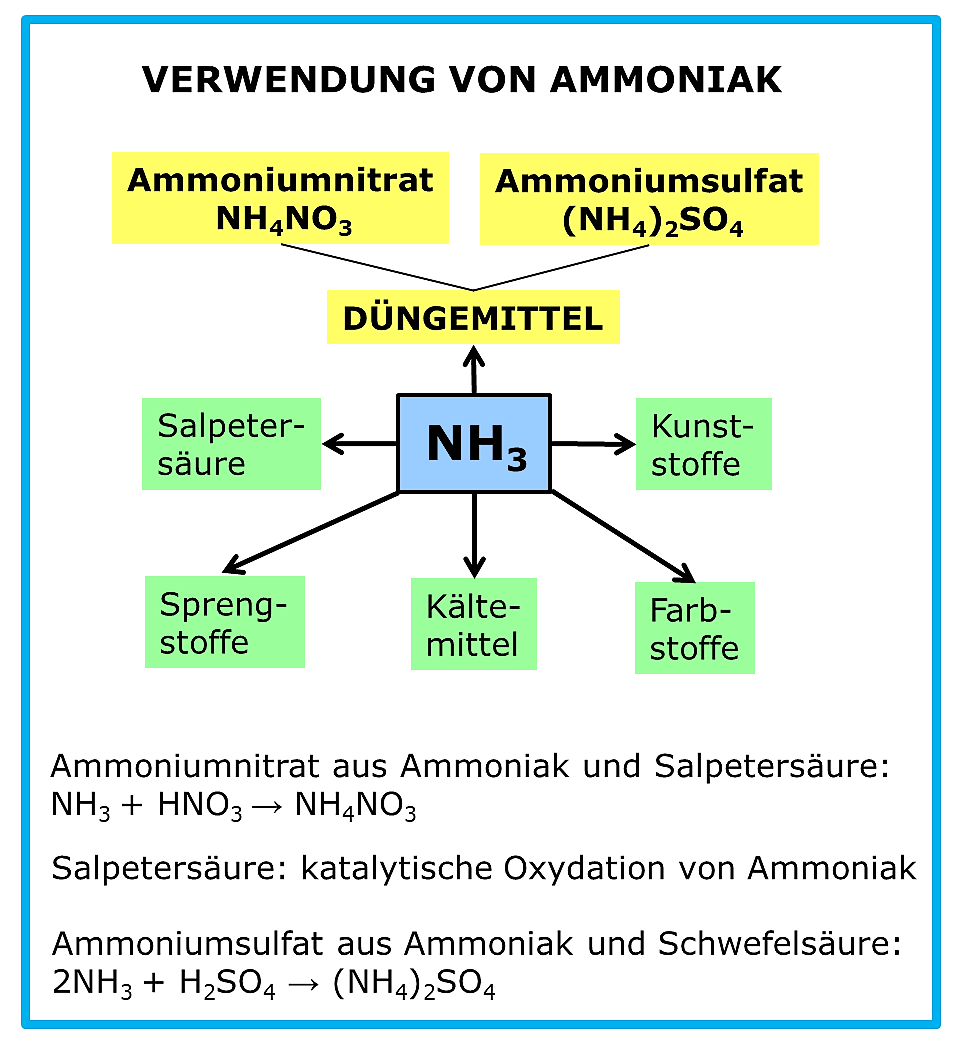
Bild 1. Ammoniak ist Ausgangsstoff für viele Produkte und hat einen ganz neuen industriellen Chemie- Zweig begründet.
Habers Forschungs- und Entwicklungsarbeit auf dem Gebiet der Ammoniak-Synthese hat sich als sehr nachhaltig erwiesen. Bis heute gibt es nichts Besseres. Die Weltproduktion von nach diesem Verfahren hergestellten Stickstoff-Dünger beträgt 100 Millionen Tonnen pro Jahr. 90% des weltweit produzierten Ammoniaks wird zur Herstellung von Düngemitteln verwandt. Das heißt, Ammoniak wird zu Ammoniumsalzen, d.h. Ammoniumsulfat und –nitrat weiter verarbeitet. Daneben ist Ammoniak Ausgangsstoff für die Produktion von Kunststoffen und Sprengstoffen. Ammoniak selbst kann als Kältemittel in Kühlanlagen eingesetzt werden und dabei die stark Umwelt gefährdenden Halogen-Kohlenwasserstoffe (FCKW und Chlorkohlenwasserstoffe) ersetzen.

Bild 2. Die Bauern, die mit Ammoniumsulfat düngen, erfreuen sich der dicksten Rüben und der saftigsten Birnen und werden dabei selbst dick und fett. Bauern, die ohne auszukommen glauben, sind dem Hungertod preisgegeben. Eine schöne alte Postkarte aus Frankreich.
Natürlich wird international laufend an der Verbesserung des Haber-Bosch-Verfahrens gearbeitet, das eine noch nicht abgeschlossene Geschichte ist.
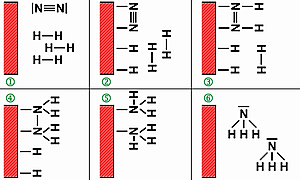
Bild 3. So arbeitet der Katalysator (rot) bei der Ammoniaksynthese: Aus N2 und H2 wird in sechs (schematischen) Stufen NH3. Es bedarf einiger Anstrengung, die stabile Dreifachbindung der Stickstoffatome aufzubrechen.
Der Katalysator. Einem Katalysator kommt die Rolle eines Heiratsvermittlers zwischen zwei Partnern zu, die ohne dessen Anwesenheit nur langsam oder gar keine Verbindung miteinander eingehen würden. Bei einer chemischen Reaktion werden zwei Ausgangsverbindungen in ein Produkt umgewandelt. Hierfür muss eine Barriere überwunden werden, vergleichbar mit einem Berg, der zwischen Start (Ausgangsverbindungen) und Ziel (Produkt) liegt. Wilhelm Ostwald: Ein Katalysator ist ein Stoff, der die Geschwindigkeit einer chemischen Reaktion erhöht, ohne selbst dabei verbraucht zu werden und ohne die endgültige Lage des thermodynamischen Gleichgewichts dieser Reaktion zu verändern.
Viele Forschungsarbeiten konzentrierten sich auf die Optimierung des Katalysators, dessen Wirkung nach wie vor recht geheimnisvoll anmutet. Wie kann man die Katalyse beschleunigen? Bis heute hat man keinen wesentlich besseren Mischkatalysator gefunden als Habers Mitarbeiter 1910. Das Problem ist nach wie vor, dass die Reaktionsgeschwindigkeit der Vereinigung von Stickstoff und Wasserstoff drastisch abnimmt, wenn die NH3-Ausbeute zunimmt: So halbiert sich z.B. die Ausbeute in Vol% NH3, wenn die Reaktionsgeschwindigkeit verdoppelt wird. Demzufolge muss das Synthesegemisch häufiger den Kreis durchlaufen, d.h. mehr Energie verbrauchen.
Die Ausgangsstoffe. Zu Habers Zeiten wurde der Wasserstoff aus Koks gewonnen und das noch bis 1960. Heute arbeiten fast alle Ammoniakanlagen auf Erdgasbasis als billigstem Ausgangsstoff. Der Wasserstoff wird aus dem Erdgas CH4 durch das Dampf-Reforming-Verfahren gewonnen. Der Energieaufwand pro Tonne NH3 liegt bei Koks als Ausgangsstoff bei 90 GJ (Gigajoule), bei Erdgas bei ca. 30 GJ.
Die Anlagengröße. Die Verwendung von Erdgas erlaubte eine wesentliche Reduzierung der Anlagengröße. So wurde innerhalb von 30 Jahren (von 1940 auf 1970) bei einer 1000-tato-Anlage (Tagestonnen) die Zahl der Reaktoren von 21 auf 1 reduziert, der Platzbedarf von 35000 m2 auf 7500 m2 verringert und der Energiebedarf gedrittelt. Das theoretische Energieminimum liegt bei 23 GJ pro Tonne NH3. Hier wäre eine weitere Verbesserung nur durch eine grundsätzlich andere Technologie, die in den Sternen steht, möglich. Für eine Tagesproduktion von 1500 Tonnen Ammoniak setzt man einen Reaktor von 2,40 m Durchmesser, 30 m Länge und einem Gewicht von ca. 400 Tonnen ein. Er fasst etwa 100 Tonnen Katalysator (heute meist Eisen mit Zusätzen von Oxiden des Calciums, Aluminiums und Siliziums sowie Kaliumcarbonat). Zur Zeit arbeitet in Deutschland nur noch eine Ammoniak-Anlage bei der BASF in Ludwigshafen, die auch nur deshalb halbwegs rentabel ist, weil sie in Bezug auf Prozessdampf und Kohlendioxid im Verbund mit anderen chemischen Produktionsanlagen im selben Werk arbeitet.
Die Probleme. Wenn die Weltbevölkerung, die 1976 4 Milliarden betrug, in den kommenden Jahrzehnten auf 8 Milliarden ansteigt, muss die Stickstoffproduktion entsprechend ausgeweitet werden. Das bedeutet einen entsprechend hohen Energieverbrauch, der letzten Endes aus fossilien Brennstoffen aufgebracht werden muss; Erdgas ist fossil, und die elektrische Energie zum Antrieb der Kompressoren stammt hauptsächlich aus fossilen Quellen. Der Haber-Bosch-Prozess ist energieintensiv, erhöht den CO2-Ausstoß und damit die Erwärmung der Atmosphäre. Er ist kapitalintensiv und technisch anspruchsvoll und damit hauptsächlich für die afrikanischen Entwicklungsländer sehr schwer zu verifizieren, wo sich obendrein die Kleinbauern den Stickstoffdünger kaum leisten können. Nach dem Ausbringen des Stickstoffdüngers bildet sich durch Einwirkung von Bakterien Nitrat, das von den Pflanzen direkt aufgenommen wird. Bei Überdüngung wird ein großer Teil des Nitrats in Flüsse ausgeschwemmt und verursacht erhebliche Umweltprobleme, z.B. Eutrophierung von Binnengewässern, das ist eine unerwünschte Zunahme an Nährstoffen im Wasser, die das ökologische Gleichgewicht stören. Das Nitrat gelangt ins Trinkwasser und kann krebserregende Nitrosamine bilden. Die denitrifizierenden Bodenbakterien emittieren Stickoxide und schädigen die schützende Ozonschicht.
Was kommt nach dem künstlichen Dünger? Es bestehen erhebliche Zweifel, dass die Erhöhung der Stickstoffdünger-Produktion die einzige Antwort auf die Welternährungsprobleme darstellt. Die andere Möglichkeit, auf die schon Haber in seiner Nobelpreisrede hingewiesen hatte, wäre die biologische Stickstofffixierung, d.h. der Versuch einer Nachahmung des Stickstoffkreislaufs, wie er in der Natur abläuft. Hier wird noch viel Arbeit notwendig sein, die für Biologen, Chemiker und Ingenieure dieser und der nächsten Generation eine sehr große Herausforderung darstellt. Um die globale Katastrophe zu vermeiden, ist die weltweite menschliche Gesellschaft aufgerufen, diese gewaltige Aufgabe zu lösen. Die Einsicht muss in die Gehirne eindringen, Probleme zwischen den Menschen niemals mit Gewalt lösen zu wollen. Wir müssen endlich, endlich aufhören, Kriege gegeneinander zu führen und endlich, endlich beginnen, den lohnenden Krieg gegen den Hunger in der Welt auf breiter Front voranzutreiben.

Bild 4. Fritz-Haber-Institut Berlin-Dahlem - Teil des "deutschen Oxford". In der Mitte des Rondells die "Haber-Linde", rechts am Rand die Haber-Villa. Bild 5. Der Lageplan: Von der physikalischen Chemie zur chemischen Physik, von der Molekülphysik zur Elektronen-Mikroskopie. K...Habers Dienstvilla ist heute Seminarraum.
Das Fritz-Haber-Institut heute. 1952 erhielt Habers Berliner Wirkungsstätte diesen Namen. 2011, zum 100-jährigen Jubiläum, war in den Medien eine Diskussion darüber entbrannt, ob das Institut, das zur Max-Planck-Gesellschaft gehört, den Namen zu Recht oder zu Unrecht erhielt. Einige Persönlichkeiten der Öffentlichkeit zeigten sich betroffen, weil es wohl nicht angehen könne, dass der Vater des Giftgaskrieges Namensgeber eines renommierten Instituts sei. Der bekannte deutsch-jüdisch-amerikanische Historiker Fritz Stern, Patensohn Fritz Habers, hielt den Festvortrag am 28. Oktober 2011. Er sagte: Selbstverständlich muss das Institut den Namen behalten. Gerade anhand der Problematik können wir den Studenten die ethische Verantwortung des Wissenschaftlers vermitteln. Mitentscheidend ist, wie man mit Haber 1933 umgegangen ist, und die Beibehaltung des Namens ist eine Wiedergutmachung nach der Vertreibung vieler jüdischer Wissenschaftler.
Bild 6. Das Gebäude der Physikalischen Chemie, im Hintergrund Fritz Habers einstige Dienstvilla.
Ähnliche Ziele wie Fritz Haber verfolgen die Wissenschaftler des Instituts noch heute. Erstens schauen sie sich die Chemie aus physikalischem Blickwinkel an: Sie untersuchen die prinzipiellen Eigenschaften von Atomen, Molekülen und Elektronen, um das Verhalten dieser Teilchen in chemischen Reaktionen zu erforschen. Zweitens wollen sie besser verstehen, wie die Strukturen von Grenzflächen, z.B. die Oberfläche eines Katalysators, chemische Reaktionen beeinflussen, um leistungsfähigere Katalysatoren für die chemische Industrie zu entwickeln. Die Erforschung der geheimnisvollen Katalyse und der molekularen Vorgänge an Oberflächen ist dabei wie ein roter Faden seit Habers Zeiten.

Bild 7. Nobelpreisträger Gerhard Ertl - in der Tradition von Fritz Haber.
Besondere Verdienste erwarb sich Gerhard Ertl (*1936, Stuttgart), Physiker und Oberflächenchemiker, der von 1986 bis 2004 Direktor der Abteilung Physikalische Chemie des Fritz-Haber-Instituts war und im Jahr 2007 den Nobelpreis für Chemie erhielt. Er hat die Entwicklung auf dem Gebiet der Oberflächenchemie maßgeblich beeinflusst. Er sagte nach der Nobelpreisverleihung: Wenn man erklärt, von Goethe nichts zu wissen, wird man mit Verachtung gestraft; wenn man sagt, nichts von Physik zu verstehen, erhält man Beifall. Das ist schlimm!
Die Abteilung für Oberflächen- und Molekülforschung des FHI beherbergt den freien Elektronenlaser, eine technische Großanlage, die den Molekülphysikern ein neues Hilfsmittel an die Hand gibt, mit denen sie den Aufbau und das Verhalten kleinster Materieteilchen auf die Spur kommen wollen.
Die Weltbevölkerung wächst, wie soll sie ernährt werden? Der englische Nationalökonom Thomas Malthus hatte schon um 1800 vorausgesagt, dass die Lebensmittelproduktion nicht mit dem Wachstum der Menschheit Schritt halten kann. Seitdem bemühten sich Forscher wie Justus von Liebig (1803-1873), die Erträge der Landwirtschaft durch künstliche Düngung zu steigern. Zwar besteht die irdische Atmosphäre zu drei Vierteln aus Stickstoff, doch in dieser elementaren Form können ihn Pflanzen nur durch Umwandlung durch bestimmte Bodenbakterien verwerten. An dieser Aufgabe bissen sich die Chemiker seit mehr als hundert Jahren die Zähne aus - bis Fritz Haber kam. Ihm gelang 1908 der große Coup: die Stickstoffdünger-Erzeugung. Seit nunmehr hundert Jahren ist es möglich, Stickstoff in Dünger zu verwandeln. Die große Überschrift über Habers Lebensleistung lautet mit Fug und Recht: Deutscher Chemiker errettet die halbe Menschheit vor dem Hungertod.
Bildnachweis.
Bild 1: Eigene Skizze. Bild 2: Wikipedia, gemeinfrei, da Schutzfrist abgelaufen. Bild 3: Wikipedia, Urheber Invexis, CC-BY-SA 3.0. Bild 4: Copyright dpa picture alliance. Bild 5, 6: Eigene Fotos 2012. Bild 7: Wikipedia, Urheber Wolfram Däumel, CC-BY-SA 3.0.